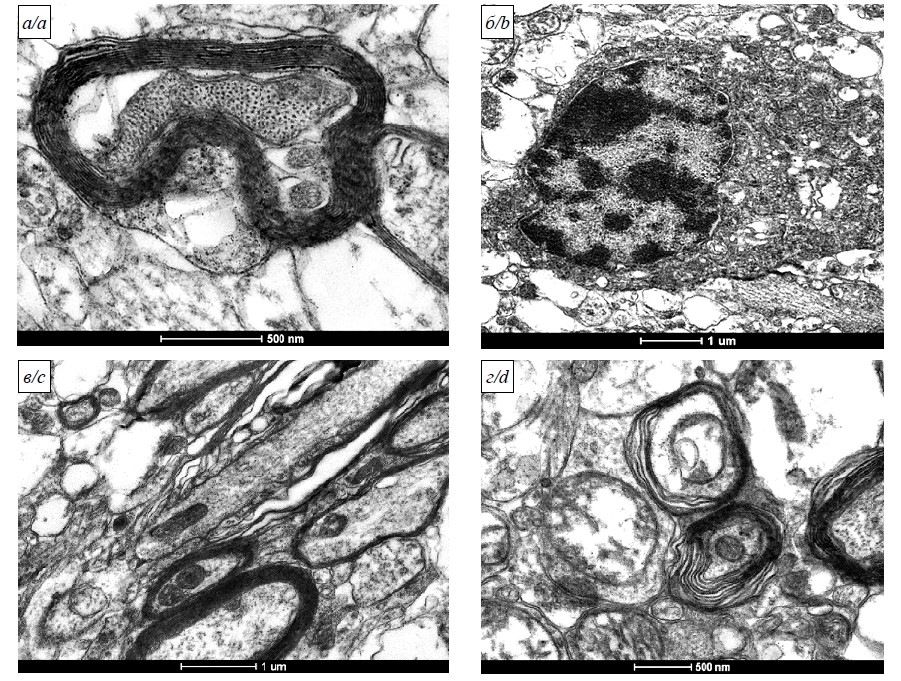
Электронно-микроскопическое исследование неокортекса сирийских хомяков (Mesocricetus auratus) при инфекции вируса SARS-CoV-2 (Coronaviridae: Coronavirinae: Betacoronavirus: Sarbecovirus)
- Авторы: Парамонова Н.М.1,2, Чепур С.В.1, Первак М.О.1, Мясников В.А.1, Тюнин М.А.1, Ильинский Н.С.1, Каневский Б.А.1, Смирнова А.В.1
-
Учреждения:
- ФГБУ «Государственный научно-исследовательский испытательный институт военной медицины» Министерства обороны Российской Федерации
- ФГБУН «Институт эволюционной физиологии и биохимии имени И.М. Сеченова» Российской академии наук
- Выпуск: Том 67, № 5 (2022)
- Страницы: 403-413
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://ogarev-online.ru/0507-4088/article/view/118237
- DOI: https://doi.org/10.36233/0507-4088-130
- ID: 118237
Цитировать
Полный текст
Аннотация
Введение. У пациентов, перенёсших COVID-19, выявляют признаки поражения центральной нервной системы, в том числе непосредственно ассоциированные с вирусом SARS-CoV-2. В связи с этим особую актуальность приобретают морфологические исследования изменений, вызываемых SARS-CoV-2, в коре головного мозга для изучения механизмов их формирования и разработки подходов к доклинической оценке эффективности противовирусных лекарственных средств.
Цель работы – изучение динамики ультраструктурных изменений в неокортексе сирийских хомяков после заражения вирусом SARS-CoV-2.
Материалы и методы. Самцов сирийских хомяков массой тела 80–100 г в возрасте 4–6 недель интраназально заражали 26 мкл культуры SARS-CoV-2 с концентрацией вирусных частиц 4×104 ТЦД50/мл. Эвтаназию выполняли на 3-и, 7-е или 28-е сутки после заражения, мозг извлекали с иссечением коры. Исследование материала проводили методом трансмиссионной электронной микроскопии.
Результаты и обсуждение. Установлено, что через трое суток после заражения в неокортексе возрастает количество умеренно гиперхромных нейронов, тогда как к 7-м суткам значимо увеличивается количество апоптотических клеток. В эти же сроки нарастают признаки нейронофагии и представительство атипичной глии. На 28-е сутки после заражения животных возрастает количество деструктивно изменённых олигодендроцитов. Показано, что вирусная инвазия уже на 3-и сутки после заражения сопряжена с конформационными изменениями клеток неокортекса – преобразованиями ядра, шероховатого эндоплазматического ретикулума и аппарата Гольджи, а также со спазмом микрососудов в сочетании с отёком периваскулярного пространства.
Заключение. В результате электронно-микроскопического исследования описаны ультраструктурные изменения неокортекса на экспериментальной модели инфекции SARS-CoV-2. Полученные данные могут быть применены для изучения патогенеза инфекции и поиска направлений разработки новых лекарственных средств.
Ключевые слова
Полный текст
Открыть статью на сайте журналаОб авторах
Наталья Михайловна Парамонова
ФГБУ «Государственный научно-исследовательский испытательный институт военной медицины» Министерства обороны Российской Федерации; ФГБУН «Институт эволюционной физиологии и биохимии имени И.М. Сеченова» Российской академии наук
Email: gniiivm_2@mil.ru
ORCID iD: 0000-0001-5451-3555
SPIN-код: 2945-3310
старший научный сотрудник
Россия, 195043, г. Санкт-Петербург; 194223, г. Санкт-ПетербургСергей Викторович Чепур
ФГБУ «Государственный научно-исследовательский испытательный институт военной медицины» Министерства обороны Российской Федерации
Email: gniiivm_2@mil.ru
ORCID iD: 0000-0002-7625-2744
SPIN-код: 3828-6730
доктор медицинских наук, профессор, начальник
Россия, 195043, г. Санкт-ПетербургМария Олеговна Первак
ФГБУ «Государственный научно-исследовательский испытательный институт военной медицины» Министерства обороны Российской Федерации
Email: gniiivm_7@mil.ru
ORCID iD: 0000-0002-1395-823X
младший научный сотрудник
Россия, 195043, г. Санкт-ПетербургВадим Александрович Мясников
ФГБУ «Государственный научно-исследовательский испытательный институт военной медицины» Министерства обороны Российской Федерации
Email: gniiivm_7@mil.ru
ORCID iD: 0000-0001-7232-4678
кандидат медицинских наук, начальник научно-исследовательского испытательного центра
Россия, 195043, г. Санкт-ПетербургМихаил Александрович Тюнин
ФГБУ «Государственный научно-исследовательский испытательный институт военной медицины» Министерства обороны Российской Федерации
Email: gniiivm_7@mil.ru
ORCID iD: 0000-0002-6974-5583
SPIN-код: 6161-7029
кандидат медицинских наук, заместитель начальника научно-исследовательского испытательного центра
Россия, 195043, г. Санкт-ПетербургНикита Сергеевич Ильинский
ФГБУ «Государственный научно-исследовательский испытательный институт военной медицины» Министерства обороны Российской Федерации
Email: nika_il2@mail.ru
ORCID iD: 0000-0001-7406-753X
SPIN-код: 5511-7800
заместитель начальника научно-исследовательского отдела
Россия, 195043, г. Санкт-ПетербургБорис Александрович Каневский
ФГБУ «Государственный научно-исследовательский испытательный институт военной медицины» Министерства обороны Российской Федерации
Email: gniiivm_7@mil.ru
ORCID iD: 0000-0002-6255-8232
SPIN-код: 2549-9294
заместитель начальника научно-исследовательского отдела
Россия, 195043, г. Санкт-ПетербургАнна Владимировна Смирнова
ФГБУ «Государственный научно-исследовательский испытательный институт военной медицины» Министерства обороны Российской Федерации
Автор, ответственный за переписку.
Email: janis_1@mail.ru
ORCID iD: 0000-0003-0483-5032
SPIN-код: 4897-0219
научный сотрудник
Россия, 195043, г. Санкт-ПетербургСписок литературы
- Чепур С.В., Плужников Н.Н., Чубарь О.В., Бакулина Л.С., Литвиненко И.В., Макаров В.А. и др. Респираторные РНК-вирусы: как подготовиться к встрече с новыми пандемическими штаммами. Успехи современной биологии. 2020; 140(4): 359–77. https://doi.org/10.31857/S0042132420040043
- Machhi J., Herskovitz J., Senan A.M., Dutta D., Nath B., Oleynikov M.D., et al. The Natural History, Pathobiology, and Clinical Manifestations of SARS-CoV-2 Infections. J. Neuroimmune Pharmacol. 2020; 15(3): 359–86. https://doi.org/10.1007/s11481-020-09944-5
- Харченко Е.П. Коронавирус SARS-CoV-2: особенности структурных белков, контагиозность и возможные иммунные коллизии. Эпидемиология и вакцинопрофилактика. 2020; 19(2): 13–30. https://doi.org/10.31631/2073-3046-2020-19-2-13-30
- Бруякин С.Д., Макаревич Д.А. Структурные белки коронавируса SARS-CoV-2: роль, иммуногенность, суперантигенные свойства и возможности использования для терапевтических целей. Вестник Волгоградского государственного медицинского университета. 2021; (2): 18–27. https://doi.org/10.19163/1994-9480-2021-2(78)-18-27
- Пащенков М.В., Хаитов М.Р. Иммунный ответ против эпидемических коронавирусов. Иммунология. 2020; 41(1): 5–18. https://doi.org/10.33029/0206-4952-2020-41-1-5-18
- Pan Y., Li X., Yang G., Fan J., Tang Y., Zhao J., et al. Serological immunochromatographic approach in diagnosis with SARS-CoV-2 infected COVID-19 patients. J. Infect. 2020; 81(1): e28–32. https://doi.org/10.1016/j.jinf.2020.03.051
- Rodríguez Y., Novelli L., Rojas M., De Santis M., Acosta-Ampudia Y., Monsalve DM., et al. Autoinflammatory and autoimmune conditions at the crossroad of COVID-19. J. Autoimmun. 2020; 114: 102506. https://doi.org/10.1016/j.jaut.2020.102506
- Nalbandian A., Sehgal K., Gupta A., Madhavan M.V., McGroder C., Stevens J.S., et al. (2021). Post-acute COVID-19 syndrome. Nat. Med. 2021; 27(4): 601–15. https://doi.org/10.1038/s41591-021-01283-z
- Mao L., Jin H., Wang M., Hu Y., Chen S., He Q., et al. Neurologic manifestations of hospitalized patients with coronavirus disease 2019 in Wuhan, China. JAMA Neurol. 2020; 77(6): 683–690. https://doi.org/10.1001/jamaneurol.2020.1127
- Pinna P., Grewal P., Hall J.P., Tavarez T., Dafer R.M., Garg R., et al. Neurological manifestations and COVID-19: Experiences from a tertiary care center at the Frontline. Journal of the neurological sciences. J. Neurol. Sci. 2020; 415: 116969. https://doi.org/10.1016/j.jns.2020.116969
- Zhou F., Yu T., Du R., Fan G., Liu Y., Liu Z., et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020; 395(10229): 1054–62. https://doi.org/10.1016/S0140-6736(20)30566-3
- Xiao A.T., Gao C., Zhang S. Profile of specific antibodies to SARS-CoV-2: The first report. J. Infect. 2020; 81(1): 147–78. https://doi.org/10.1016/j.jinf.2020.03.012
- Logunov D.Y., Dolzhikova I.V., Shcheblyakov D.V., Tukhvatulin A.I., Zubkova O.V., Dzharullaeva A.S., et al. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia. Lancet. 2021; 397(10275): 671–81. https://doi.org/10.1016/S0140-6736(21)00234-8
- Jones I., Roy P. Sputnik V COVID-19 vaccine candidate appears safe and effective. Lancet. 2021; 397(10275): 642–3. https://doi.org/10.1016/S0140-6736(21)00191-4
- Dassarma B., Tripathy S., Matsabisa M. Emergence of ancient convalescent plasma (CP) therapy: to manage COVID-19 pandemic. Transfus. Clin. Biol. 2021; 28(1): 123–127. https://doi.org/10.1016/j.tracli.2020.11.004
- Chakraborty C., Sharma A.R., Sharma G., Bhattacharya M., Lee S.S. SARS-CoV-2 causing pneumonia-associated respiratory disorder (COVID-19): diagnostic and proposed therapeutic options. Eur. Rev. Med. Pharmacol. Sci. 2020; 24(7): 4016–26. https://doi.org/10.26355/eurrev_202004_20871
- Wu X., Yu K., Wang Y., Xu W., Ma H., Hou Y., et al. Efficacy and safety of Triazavirin therapy for coronavirus disease 2019: a pilot randomized controlled trial. Engineering (Beijing). 2020; 6(10): 1185–91. https://doi.org/10.1016/j.eng.2020.08.011
- Chan J.F.W., Zhang A.J., Yuan S., Poon V.K.M., Chan C.C.S., Lee A.C.Y., et al. Simulation of the clinical and pathological manifestations of coronavirus disease 2019 (COVID-19) in a golden Syrian hamster model: implications for disease pathogenesis and transmissibility. Clin. Infect. Dis. 2020; 71(9): 2428–46. https://doi.org/10.1093/cid/ciaa325
- TaŞtan C., Yurtsever B., Sir KarakuŞ G., Dİlek KanÇaĞi D., Demİr S., Abanuz S., et al. SARS-CoV-2 isolation and propagation from Turkish COVID-19 patients. Turk. J. Biol. 2020; 44(3): 192–202. https://doi.org/10.3906/biy-2004-113
- Yao P., Zhang Y., Sun Y., Gu Y., Xu F., Su B., et al. Isolation and growth characteristics of SARS-CoV-2 in vero cell. Virol. Sin. 2020; 35(3): 348–50. https://doi.org/10.1007/s12250-020-00241-2
- Reed L.J., Muench H. A simple method of estimating fifty percent endpoints. Am. J. Hygiene. 1938; 27: 493–7. https://doi.org/10.1093/oxfordjournals.aje.a118408
- Макаренко И.Е., Авдеева О.И., Ванатиев Г.В., Рыбакова А.В., Ходько С.В., Макарова М.Н. и др. Возможные пути и объемы введения лекарственных средств лабораторным животным. Международный вестник ветеринарии. 2013; (3): 72–84.
- Гайер Г., ред. Электронная гистохимия. Пер. с нем. М.: Мир; 1974.
- Saraste J., Prydz K. Assembly and cellular exit of coronaviruses: hijacking an unconventional secretory pathway from the pre-Golgi intermediate compartment via the golgi ribbon to the extracellular space. Cells. 2021; 10(3): 503. https://doi.org/10.3390/cells10030503
- Hackstadt T., Chiramel A.I., Hoyt F.H., Williamson B.N., Dooley C.A., Beare P.A., et al. Disruption of the Golgi apparatus and contribution of the endoplasmic reticulum to the SARS-CoV-2 replication complex. Viruses. 2021; 13(9): 1798. https://doi.org/10.3390/v13091798
- Чепур С.В., Мясников В.А., Тюнин М.А., Ильинский Н.С., Никишин А.С., Исаева А.А. и др. Модель новой коронавирусной инфекции у золотистых сирийских хомячков: основные патологические изменения. Биомедицина. 2021; 17(3): 90–4. https://doi.org/10/33647/2074-5982-17-3-90-94
- Чепур С.В., Тюнин М.А., Мясников В.А., Алексеева И.И., Владимирова О.О., Ильинский Н.С. и др. Поражение органов и тканей SARS-CoV-2: биологическая модель на сирийских хомяках Mesocricetus auratus для экспериментальных (доклинических) исследований. Клиническая и экспериментальная морфология. 2021; 10(4): 25–34. https://doi.org/10.31088/CEM2021.10.4.25-34
- Billioux B.J., Smith B., Nath A. Neurological complications of Ebola virus infection. Neurotherapeutics. 2016; 13(3): 461–70. https://doi.org/10.1007/s131311-016-0457-z
- Чепур С.В., Плужников Н.Н., Сайганов С.А., Бакулина Л.С., Чубарь О.В., Юдин М.А. и др. Гипотеза матричного синтеза апериодических полисахаридов. Успехи современной биологии. 2019; 139(6): 583–93. https://doi.org/10.1134/S0042132419060012
- Sinha N., Balayla G. Hydroxychloroquine and COVID-19. Postgrad. Med. J. 2020; 96(1139): 550–5. https://doi.org/10.1136/postgradmedj-2020-137785
Дополнительные файлы