Study of the teratogenicity of the vaccine strain of the Rubella virus «Orlov-V» (Matonaviridae: Rubivirus: Rubella virus) in experience on rhesus macaques
- Authors: Lavrentjeva I.N.1, Shamsutdinova O.A.2, Chugueva I.I.2, Karal-ogly D.D.2, Vyshemirskiy O.I.2
-
Affiliations:
- FSBI «Saint Petersburg Pasteur Research Institute of Epidemiology and Microbiology» of the Federal Service for Surveillance on Consumer Rights Protection and Human Wellbeing
- FSBRI «Research Institute of Medical Primatology» of the Ministry of Education and Science of Russia
- Issue: Vol 65, No 6 (2020)
- Pages: 357-363
- Section: ORIGINAL RESEARCHES
- URL: https://ogarev-online.ru/0507-4088/article/view/118154
- DOI: https://doi.org/10.36233/0507-4088-2020-65-6-6
- ID: 118154
Cite item
Abstract
Introduction. Rubella virus has pronounced teratogenic properties that can cause generalized and persistent intrauterine infection of the fetus. As a result, the control of the loss of teratogenicity inherent in «wild-type» virus strains is a necessary stage of a preclinical study of the vaccine strain for a live attenuated rubella vaccine.
The purpose of the study is to comprehensively study the teratogenic properties of the vaccine strain of rubella virus «Orlov-V» in the experiment on rhesus macaques.
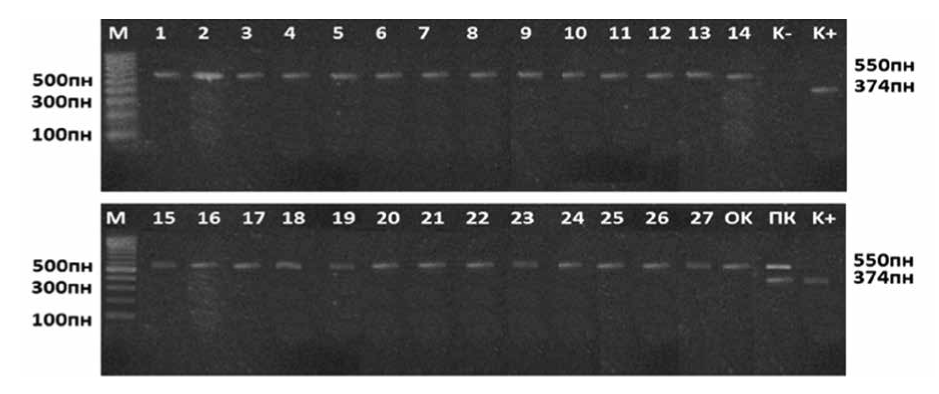
Material and methods. Seronegative to rubella virus female rhesus macaques in early pregnancy at the age of 4–7 years (n = 13) were used in the experiment. Animals of the experimental group (n = 9) received single immunization intramuscularly with a preparation from the «Orlov-V» strain. The control group of the monkeys (n = 3) were immunized with a commercial vaccine containing Wistar RA27/3 strain. The female of the control group (n = 1) was injected with a solvent used in the rubella vaccine. Study of possible teratogenic properties of vaccine strains of rubella virus was carried out using a complex of clinical, immunological, pathomorphological and virological methods. Clinical observations were made within 3 months after the monkeys’ birth. Determination of antibody titers in the blood serum of immunized monkeys was performed in HI test on the 28th–30th day after infection. The ELISA method was applied to determine IgM antibodies in the blood serum of newborns within the first month of life. Detection of rubella virus RNA was performed by PCR with electrophoretic detection of amplicons.
Results. No markers of congenital rubella infection were found in infants born from monkeys vaccinated during the pregnancy. It is shown that PCR can be an informative method to confirm the absence of teratogenic properties of vaccine strains of rubella virus.
Discussion. The obtained data demonstrated that vaccine strains of the «Orlov-V» rubella virus and Wistar RA27/3 have lost their teratogenic properties. The possibility of using an alternative strategy for preclinical assessment of specific safety of antiviral vaccines including a complex of clinical, immunological, pathologic and virological methods instead of the classical pathologic method is discussed.
Conclusion. The results obtained in this study showed the absence of teratogenic properties and high immunogenic activity of the vaccine strain of rubella virus «Orlov-V».
Full Text
##article.viewOnOriginalSite##About the authors
I. N. Lavrentjeva
FSBI «Saint Petersburg Pasteur Research Institute of Epidemiology and Microbiology» of the Federal Service for Surveillance on Consumer Rights Protection and Human Wellbeing
Email: pasteur.lawr@mail.ru
ORCID iD: 0000-0002-2188-6547
Ph.D. Doctor of medical Sciences, head of laboratory of experimental virology
197101, Saint-Petersburg
Russian FederationO. A. Shamsutdinova
FSBRI «Research Institute of Medical Primatology» of the Ministry of Education and Science of Russia
Author for correspondence.
Email: shamsutdinova-o-a@yandex.ru
ORCID iD: 0000-0002-2742-3965
scientist, lab. immunology and cell biology
Sochi, 354376
Russian FederationI. I. Chugueva
FSBRI «Research Institute of Medical Primatology» of the Ministry of Education and Science of Russia
Email: Chuguevairina@mail.ru
ORCID iD: 0000-0002-1567-1929
veterinarian
Sochi, 354376
Russian FederationD. D. Karal-ogly
FSBRI «Research Institute of Medical Primatology» of the Ministry of Education and Science of Russia
Email: karal_5@mail.ru
ORCID iD: 0000-0003-3606-1668
Ph.D. leading scientist, lab. immunology and cell biology
Sochi, 354376
Russian FederationO. I. Vyshemirskiy
FSBRI «Research Institute of Medical Primatology» of the Ministry of Education and Science of Russia
Email: olegvyshem@mail.ru
ORCID iD: 0000-0002-5345-8926
Ph.D. leading scientist, lab. infectious virology
Sochi, 354376
Russian FederationReferences
- Castillo-Solórzano C., Reef S.E., Morice A., Vascones N., Chevez A.E., Castalia-Soares R., et al. Rubella vaccination of unknowingly pregnant women during mass campaigns for rubella and congenital rubella syndrome elimination, the Americas 2001–2008. J. Infect. Dis. 2011; 204 (Suppl. 2): S713–7. https://doi.org/10.1093/infdis/jir489.
- Шамсутдинова О.А. Живые аттенуированные вакцины для иммунопрофилактики. Инфекция и иммунитет. 2017; 7(2): 107–16. https://doi.org/10.15789/2220-7619-2017-2-107-116.
- Hofmann J., Kortung M., Pustowoit B., Faber R., Piskazeck U., Liebert U.G. Persistent fetal rubella vaccine virus infection following inadvertent vaccination during early pregnancy. J. Med. Virol. 2000; 61(1): 155–8. https://doi.org/10.1002/(sici)1096-9071(200005)61:1%3C155::aid-jmv25%3E3.0.co;2-o.
- Da Silva e Sá G.R., Camacho L.A., Stavola M.S., Lemos X.R., Basílio de Oliveira C.A., Siqueira M.M. Pregnancy outcomes following rubella vaccination: A prospective study in the State of Rio de Janeiro, Brazil, 2001–2002. J. Infect. Dis. 2011; 204(2):S722–8. https://doi.org/10.1093/infdis/jir408.
- Keller-Stanislawski B., Englun J.A., Kang G., Mangtani P., Neuzil K., Nohynek H., et al. Safety of immunization during pregnancy: A review of the evidence of selected inactivated and live attenuated vaccines. Vaccine. 2014; 32(52): 7057–64. https://doi.org/10.1016/j.vaccine.2014.09.052.
- Hamkar R., Jalilvand S., Abdolbaghi M.H., Esteghamati A.R., Hagh-Goo A., Jelyani K.N., et al. Inadvertent rubella vaccination of pregnant women: Evaluation of possible transplacental infection with rubella vaccine. Vaccine. 2006; 24(17): 3558–63. https://doi.org/10.1016/j.vaccine.2006.02.001.
- Mangtani P., Evans S.J.W., Lange B., Oberle D., Smith J., Drechsel- Baeuerle U., et al. Safety profile of rubella vaccine administered to pregnant women: A systematic review of pregnancy related adverse events following immunisation, including congenital rubella syndrome and congenital rubella infection in the foetus or infant. Vaccine. 2020; 38(5): 963–78. https://doi.org/10.1016/j.vaccine.2019.11.070.
- Regan A.K. The safety of maternal immunization. Hum. Vacc. Immunother. 2016; 12(12): 3132–6. https://doi.org/10.1080/21645515.2016.1222341.
- Nasiri R., Yoseffi J., Khajedaloe M., Sarafraz Yazdi M., Delgoshaei F. Congenital rubella syndrome after rubella vaccination in 1–4 weeks periconceptional period. Indian J. Pediatr. 2009; 76(3): 279–82. https://doi.org/10.1007/s12098-009-0053-x.
- Миронов А.Н., Бунатян Н.Д. Руководство по проведению до- клинических исследований лекарственных средств. Том 1. М.: Гриф и К; 2012.
- СП 3.3.2.561-96. Государственные испытания и регистрация новых иммунобиологических препаратов. М.: 1998.
- Knipe D.M., Howley P.M., eds. Fields Virology. Philadelphia: Williams & Wilkins; 2013.
- Лаврентьева И.Н. Молекулярно-биологические свойства аттенуированных штаммов вируса краснухи. Журнал микробиологии, эпидемиологии и иммунобиологии. 2008; 85(4): 55–9.
- Лаврентьева И.Н., Сухобаевская Л.П., Жебрун А.Б. Штамм вируса краснухи для получения медицинских иммунобиологических препаратов (МИБП). Патент РФ №2081912; 1995.
- Miller E., Cradock-Watson J.E., Pollock T.M. Consequences of confirmed maternal rubella at successive stage of pregnancy. Lancet. 1982; 2(8302): 781–4. https://doi.org/10.1016/s0140-6736(82)92677-0.
- Yazigi A., Eldin De Pecoulas A., Vauloup-Fellous C., Grangeot- Keros L., Ayoubi J.M., Picone O. Fetal and neonatal abnormalities due to congenital rubella syndrome: a review of literature. J. Matern. Fetal Neonatal Med. 2017; 30(3): 274–8. https://doi.org/10.3109/14767058.2016.1169526.
- Best J.M. Rubella. Semin. Fetal Neonat. Med. 2007; 12(3): 182–92. https://doi.org/10.1016/j.siny.2007.01.017.
- Sampedro Martínez A., Martínez L.A., Teatino P.M., Rodríguez- Granger J. Diagnosis of congenital infection. Enferm. Infecc. Microbiol. Clin. 2011; 29 (Suppl. 5): 15–20. https://doi.org/10.1016/s0213-005x(11)70039-8 (in Spanish).
- Macе M., Cointe D., Six C., Levy-Bruhl D., Parent du Chatelet I., Ingrand D., et al. Assessment of the diagnostic value of RT-PCR on amniotic fluid for prenatal diagnosis of congenital rubella infection. Pathol. Biol. (Paris). 2004; 52(9): 540–3. https://doi.org/10.1016/j.patbio.2004.06.004 (in French).
Supplementary files