Объективные критерии МРТ-оценки эффективности лечения метастазов в кости у больных раком предстательной железы и раком молочной железы: систематический обзор и метаанализ
- Авторы: Рипп В.О.1, Березовская Т.П.1, Иванов С.А.1
-
Учреждения:
- Медицинский радиологический научный центр имени А.Ф. Цыба — филиал федерального государственного бюджетного учреждения, «Национальный медицинский исследовательский центр радиологии» Министерства здравоохранения Российской Федерации
- Выпуск: Том 2, № 3 (2021)
- Страницы: 289-300
- Раздел: Систематические обзоры
- URL: https://ogarev-online.ru/DD/article/view/77311
- DOI: https://doi.org/10.17816/DD77311
- ID: 77311
Цитировать
Аннотация
Обоснование. Возможность персонифицированного подхода к лечению метастатического рака предстательной железы (РПЖ) и рака молочной железы (РМЖ) требует объективных методов оценки ответа на лечение очагов в скелете. Доказанная высокая эффективность МРТ в выявлении метастазов в кости в сочетании с отсутствием ионизирующего излучения создаёт предпосылки для использования метода в мониторировании хода лечения на основе объективных критериев оценки терапевтического эффекта.
Цель ― оценить возможности объективных количественных и полуколичественных МРТ-критериев в определении эффективности лечения (радио-, химио-, гормоно- и таргетная терапия) метастазов в кости, применявшихся в клинических исследованиях у больных РПЖ и РМЖ.
Материалы и методы. Поиск в базах данных Embase, PubMed, Cochrane Central Register of Controlled trials (CENTRAL), eLibrary осуществлялся до 01.06.2021 по ключевым словам «magnetic resonance imaging», «MRI», «DWI», «treatment response», «prostate cancer», «breast cancer», «bone metastasis» на английском и русском языках. В обзор включали только исследования по объективной МРТ-оценке эффективности любого типа лечебного воздействия (за исключением хирургии) при метастатическом поражении скелета.
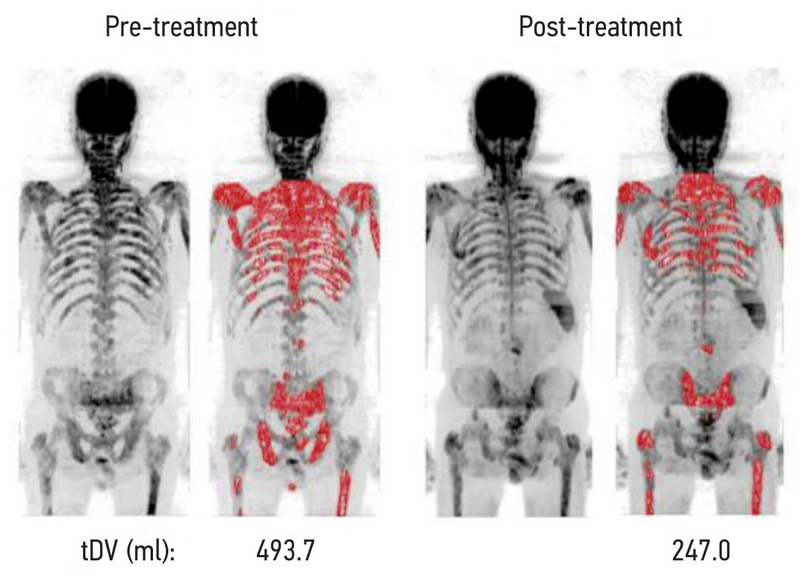
Результаты. На основании анализа 11 исследований, отобранных из 312 источников, выделены 4 группы объективных МРТ-критериев оценки терапевтического эффекта при метастатическом поражении костей у больных РПЖ и РМЖ, включающих динамику размеров, интенсивности сигнала на диффузионно-взвешенном изображении, числовых значений измеряемого коэффициента диффузии (ИКД), общей опухолевой нагрузки. Изменения этих количественных и полуколичественных показателей во всех работах, за единственным исключением, имели одинаковую направленность, хотя и различались числовыми значениями. Учитывая статистически значимую гетерогенность (p <0,1 для критерия χ2 и при I2 >40%) для значений ИКД до и после лечения, для анализа использовалась модель случайных эффектов. Изменение ИКД в результате лечения в среднем составило +0,35 [+0,12; +0,49] ×10-3 мм2/с со средними значениями ИКД до лечения 0,83 [0,71; 1,03] ×10-3 мм2/с, после лечения ― 1,18 [0,83; 1,49] ×10-3 мм2/с.
Заключение. МРТ является информативной методикой для объективной оценки ответа костных метастазов на терапию у больных РПЖ и РМЖ на основе количественных и полуколичественных критериев и имеет значительный потенциал в качестве диагностического инструмента для мониторирования эффективности лечения метастатического поражения скелета.
Полный текст
Открыть статью на сайте журналаОб авторах
Владислав Олегович Рипп
Медицинский радиологический научный центр имени А.Ф. Цыба — филиал федерального государственного бюджетного учреждения, «Национальный медицинский исследовательский центр радиологии» Министерства здравоохранения Российской Федерации
Email: rippnba@gmail.com
ORCID iD: 0000-0001-8970-4212
Врач-рентгенолог
Россия, 249036, Обнинск, ул. Королева, д. 4Татьяна Павловна Березовская
Медицинский радиологический научный центр имени А.Ф. Цыба — филиал федерального государственного бюджетного учреждения, «Национальный медицинский исследовательский центр радиологии» Министерства здравоохранения Российской Федерации
Email: berez@mrrc.obninsk.ru
ORCID iD: 0000-0002-3549-4499
главный научный сотрудник отделения МРТ, доктор медицинских наук, профессор
249036, Обнинск, ул. Королева, д. 4Сергей Анатольевич Иванов
Медицинский радиологический научный центр имени А.Ф. Цыба — филиал федерального государственного бюджетного учреждения, «Национальный медицинский исследовательский центр радиологии» Министерства здравоохранения Российской Федерации
Автор, ответственный за переписку.
Email: oncourolog@gmail.com
ORCID iD: 0000-0001-7689-6032
директор МРНЦ им А.Ф. Цыба, доктор медицинских наук, профессор РАН
Россия, 249036, Обнинск, ул. Королева, д. 4Список литературы
- Lecouvet F.E., Larbi A., Pasoglou V., et al. MRI for response assessment in metastatic bone disease//Eur Radiol. 2013. Vol. 23, N 7. Р. 1986–1997. doi: 10.1007/s00330-013-2792-3
- Padhani A.R., Makris A., Gall P., et al. Therapy monitoring of skeletal metastases with whole-body diffusion MRI//J Magn Reson Imaging. 2014. Vol. 39, N 5. Р. 1049–1078. doi: 10.1002/jmri.24548
- Woolf D.K., Padhani A.R., Makris A. Assessing response to treatment of bone metastases from breast cancer: what should be the standard of care?//Ann Oncol. 2015. Vol. 26, N 6. Р. 1048–1057. doi: 10.1093/annonc/mdu558
- Padhani A.R., Gogbashian A. Bony metastases: assessing response to therapy with whole-body diffusion MRI//Cancer Imaging. 2011. Vol. 11, N 1A. Р. S129–S145. doi: 10.1102/1470-7330.2011.9034
- Byun W.M., Shin S.O., Chang Y., et al. Diffusion-weighted MR imaging of metastatic disease of the spine: assessment of response to therapy//AJNR Am J Neuroradiol. 2002. Vol. 23, N 6. Р. 906–912.
- Padhani A.R., Lecouvet F.E., Tunariu N., et al. METastasis reporting and data system for prostate cancer: practical guidelines for acquisition, interpretation, and reporting of whole-body magnetic resonance imaging-based evaluations of multiorgan involvement in advanced prostate cancer//Eur Urol. 2017. Vol. 71, N 1. Р. 81–92. doi: 10.1016/j.eururo.2016.05.033
- Zugni F., Ruju F., Pricolo P., et al. The added value of whole-body magnetic resonance imaging in the management of patients with advanced breast cancer//PLoS One. 2018. Vol. 13, N 10. Р. e0205251. doi: 10.1371/journal.pone.0205251
- Yang H.L., Liu T., Wang X.M., et al. Diagnosis of bone metastases: a meta-analysis comparing ¹⁸FDG PET, CT, MRI and bone scintigraphy//Eur Radiol. 2011. Vol. 21, N 12. Р. 2604–2617. doi: 10.1007/s00330-011-2221-4
- Messiou C., Collins D.J., Giles S., et al. Assessing response in bone metastases in prostate cancer with diffusion weighted MRI//Eur Radiol. 2011. Vol. 21, N 10. 2169–2177. doi: 10.1007/s00330-011-2173-8
- Reischauer C., Froehlich J.M., Koh D.M., et al. Bone metastases from prostate cancer: assessing treatment response by using diffusion-weighted imaging and functional diffusion maps ― initial observations//Radiology. 2010. Vol. 257, N 2. Р. 523–531. doi: 10.1148/radiol.10092469
- Perez-Lopez R., Mateo J., Mossop H., et al. Diffusion-weighted imaging as a treatment response biomarker for evaluating bone metastases in prostate cancer: a pilot study//Radiology. 2017. Vol. 283, N 1. Р. 168–177. doi: 10.1148/radiol.2016160646
- Blackledge M.D., Collins D.J., Tunariu N., et al. Assessment of treatment response by total tumor volume and global apparent diffusion coefficient using diffusion-weighted MRI in patients with metastatic bone disease: a feasibility study//PLoS One. 2014. Vol. 9, N 4. Р. e91779. doi: 10.1371/journal.pone.0091779
- Liberati A., Altman D.G., Tetzlaff J., et al. The PRISMA statement for reporting systematic reviews and meta-analyses of studies that evaluate health care interventions: explanation and elaboration//PLoS Med. 2009. Vol. 6, N 7. Р. e1000100. doi: 10.1371/journal.pmed.1000100
- Amir-Behghadami M., Janati A. Population, Intervention, Comparison, Outcomes and Study (PICOS) design as a framework to formulate eligibility criteria in systematic reviews//Emerg Med J. 2020. Vol. 37, N 6. Р. 387. doi: 10.1136/emermed-2020-209567
- Whiting P.F. QUADAS-2: a revised tool for the quality assessment of diagnostic accuracy studies//Ann Intern Med. 2011. Vol. 155, N 8. Р. 529–536. doi: 10.7326/0003-4819-155-8-201110180-00009
- Сергеев Н.И., Котляров П.М., Солодкий В.А. Диффузионно-взвешенная магнитно-резонансная томография в оценке химиолучевого лечения метастатического поражения костных структур//Вестник Российского научного центра рентгенорадиологии Минздрава России. 2016. Т. 16, № 3. С. 2.
- Çiray I., Lindman H., Åström K.G., et al. early response of breast cancer bone metastases to chemotherapy evaluated with mr imaging//Acta Radiologica. 2001. Vol. 42, N 2. Р. 198–206. doi: 10.1080/028418501127346503
- Brown A.L., Middleton G., Macvicar A.D., et al. T1-weighted magnetic resonance imaging in breast cancer vertebral metastases: Changes on treatment and correlation with response to therapy//Clin Radiol. 1998. Vol. 53, N 7. Р. 493–501. doi: 10.1016/s0009-9260(98)80168-2
- Tombal B., Rezazadeh A., Therasse P., et al. Magnetic resonance imaging of the axial skeleton enables objective measurement of tumor response on prostate cancer bone metastases//Prostate. 2005. Vol. 65, N 2. Р. 178–187. doi: 10.1002/pros.20280
- Cappabianca S., Capasso R., Urraro F., et al. Assessing response to radiation therapy treatment of bone metastases: short-term followup of radiation therapy treatment of bone metastases with diffusion-weighted magnetic resonance imaging//J Radiotherapy. 2014. doi: 10.1155/2014/698127
- Котляров П.М., Сергеев Н.И., Федина О.Н. МРТ в диагностике метастатического поражения скелета и в оценке эффективности лечения//Радиология практика. 2006. № 6. С. 10–15.
- Lecouvet F.E., Talbot J.N., Messiou C., et al. Monitoring the response of bone metastases to treatment with Magnetic Resonance Imaging and nuclear medicine techniques: A review and position statement by the European Organisation for Research and Treatment of Cancer imaging group//Eur J Cancer. 2014. Vol. 50, N 15. Р. 2519–2531. doi: 10.1016/j.ejca.2014.07.002
- Grimm R., Padhani A.R. Whole-body diffusion-weighted MR image analysis with syngo.via frontier MR total tumor//Magn Flash. 2017. Vol. 68, N 2. Р. 73–75.
- Jambor I., Kuisma A., Ramadan S., et al. Prospective evaluation of planar bone scintigraphy, SPECT, SPECT/CT, 18F-NaF PET/CT and whole body 1.5T MRI, including DWI, for the detection of bone metastases in high risk breast and prostate cancer patients: SKELETA clinical trial//Acta Oncol. 2016. Vol. 55, N 1. Р. 59–67. doi: 10.3109/0284186X.2015.1027411
- Heusner T.A., Kuemmel S., Koeninger A., et al. Diagnostic value of diffusion-weighted magnetic resonance imaging (DWI) compared to FDG PET/CT for whole-body breast cancer staging//Eur J Nucl Med Mol Imaging. 2010. Vol. 37, N 6. Р. 1077–1086. doi: 10.1007/s00259-010-1399-z
- Eisenhauer E.A., Therasse P., Bogaerts J., et al. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1)//Eur J Cancer. 2009. Vol. 45, N 2. Р. 228–247. doi: 10.1016/j.ejca.2008.10.026
- Costelloe C.M., Chuang H.H., Madewell J.E., et al. Cancer response criteria and bone metastases: RECIST 1.1, MDA and PERCIST//J Cancer. 2010. Vol. 1. Р. 80–92. doi: 10.7150/jca.1.80
Дополнительные файлы