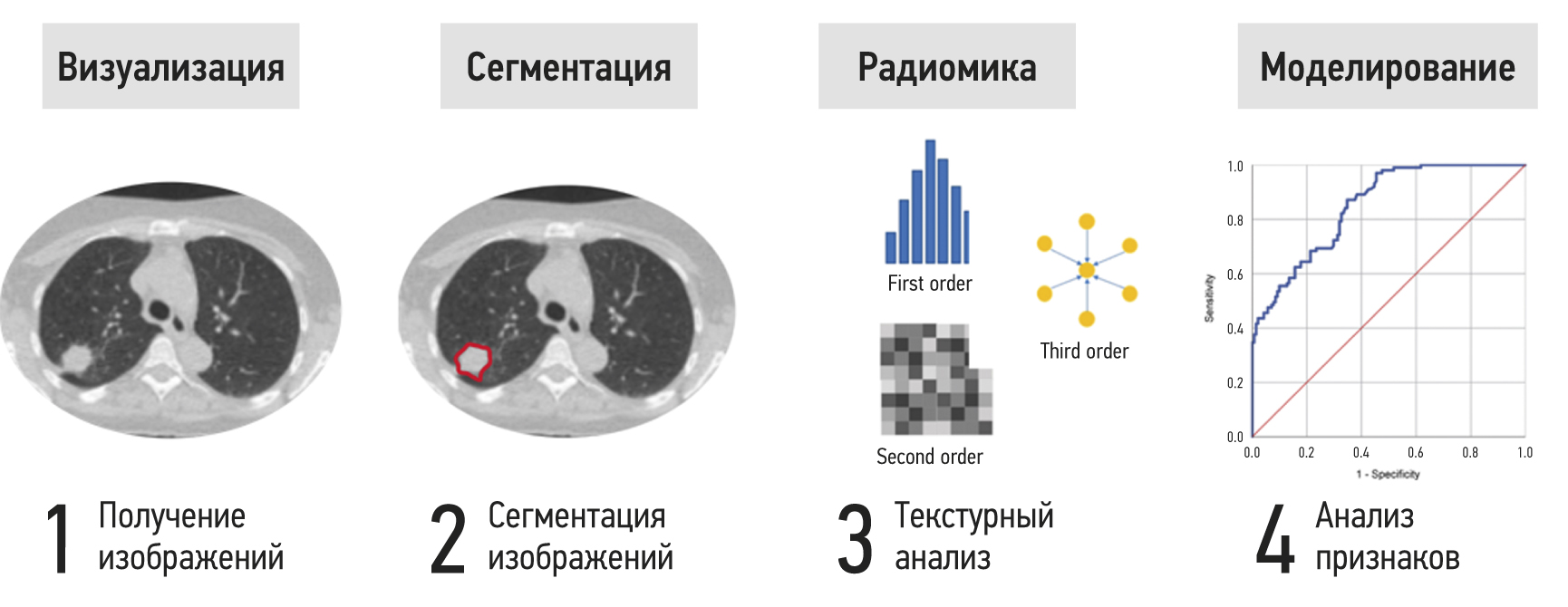
Дозиомика в анализе медицинских изображений и перспективы её использования в клинической практике
- Авторы: Солодкий В.А.1, Нуднов Н.В.1, Иванников М.Е.1, Шахвалиева Э.С.1, Сотников В.М.1, Смыслов А.Ю.1
-
Учреждения:
- Российский научный центр рентгенорадиологии
- Выпуск: Том 4, № 3 (2023)
- Страницы: 340-355
- Раздел: Систематические обзоры
- URL: https://ogarev-online.ru/DD/article/view/254073
- DOI: https://doi.org/10.17816/DD420053
- ID: 254073
Цитировать
Аннотация
Обоснование. В последние годы увеличивается количество статей с использованием термина «дозиомика», однако литературные обзоры на русском языке по данной теме отсутствуют.
Цель настоящего обзора ― описать основные принципы дозиомики как направления радиомики и проанализировать исследования по оценке возможностей применения их в клинической практике.
Материалы и методы. Систематический поиск литературы был произведён в базе данных PubMed с поисковым запросом «dosiomics OR dosiomic», а также в базе данных eLibrary с поисковым запросом «дозиомика». По состоянию на апрель 2023 года были опубликованы 43 зарубежных исследования на тему использования дозиомики в клинической практике и одна отечественная работа с определением термина «дозиомика».
Результаты. Проанализированы 43 зарубежных исследования на тему использования дозиомики в клинической практике и 1 отечественная статья с определением термина «дозиомика». Проанализированные работы разделены на три группы согласно их тематике и составлены таблицы, описывающие результаты 27 исследований по прогнозированию клинических исходов.
Заключение. В настоящее время дозиомика является новым и перспективным направлением радиомики, применяемым в текстурном анализе медицинских изображений, связанных с лучевым лечением онкологических больных. Дозиомика может способствовать развитию более персонализированного подхода к планированию лучевой терапии, прогнозированию лучевых повреждений нормальных тканей и диагностике рецидивов.
Полный текст
Открыть статью на сайте журналаОб авторах
Владимир Алексеевич Солодкий
Российский научный центр рентгенорадиологии
Email: direktor@rncrr.ru
ORCID iD: 0000-0002-1641-6452
SPIN-код: 9556-6556
д-р мед. наук, профессор, академик РАН
Россия, МоскваНиколай Васильевич Нуднов
Российский научный центр рентгенорадиологии
Автор, ответственный за переписку.
Email: nudnov@rncrr.ru
ORCID iD: 0000-0001-5994-0468
SPIN-код: 3018-2527
д-р мед. наук, профессор
Россия, МоскваМихаил Евгеньевич Иванников
Российский научный центр рентгенорадиологии
Email: ivannikovmichail@gmail.com
ORCID iD: 0009-0007-0407-0953
Россия, Москва
Элина Саид-Аминовна Шахвалиева
Российский научный центр рентгенорадиологии
Email: shelina9558@gmail.com
ORCID iD: 0009-0000-7535-8523
Россия, Москва
Владимир Михайлович Сотников
Российский научный центр рентгенорадиологии
Email: vmsotnikov@mail.ru
ORCID iD: 0000-0003-0498-314X
SPIN-код: 3845-0154
д-р мед. наук, профессор
Россия, МоскваАлексей Юрьевич Смыслов
Российский научный центр рентгенорадиологии
Email: smyslov.ay@gmail.com
ORCID iD: 0000-0002-6409-6756
SPIN-код: 9341-0037
канд. тех. наук
Россия, МоскваСписок литературы
- Arroyo-Hernández M., Maldonado F., Lozano-Ruiz F., et al. Radiation-induced lung injury: Current evidence // BMC Pulm Med. 2021. Vol. 21, N 1. P. 1–12. doi: 10.1186/s12890-020-01376-4
- Huang Y., Feng A., Lin Y., et al. Radiation pneumonitis prediction after stereotactic body radiation therapy based on 3D dose distribution: Dosiomics and/or deep learning-based radiomics features // Radiat Oncol. 2022. Vol. 17, N 1. P. 188. doi: 10.1186/s13014-022-02154-8
- Morelli L., Parrella G., Molinelli S., et al. A dosiomics analysis based on linear energy transfer and biological dose maps to predict local recurrence in sacral chordomas after carbon-ion radiotherapy // Cancers. 2023. Vol. 15, N 1. P. 33. doi: 10.3390/cancers15010033
- Ryan S.M., Fingerlin T.E., Mroz M., et al. Radiomic measures from chest high-resolution computed tomography associated with lung function in sarcoidosis // Eur Respir J. 2021. Vol. 54, N 2. P. 1900371. doi: 10.1183/13993003.00371-2019
- Hooda R., Mittal A., Sofat S. Segmentation of lung fields from chest radiographs: A radiomic feature-based approach // Biomed Eng Lett. 2019. Vol. 9, N 1. P. 109–117. doi: 10.1007/s13534-018-0086-z
- Zhang B., Ni-Jia-Ti M.Y., Yan R., et al. CT-based radiomics for predicting the rapid progression of coronavirus disease 2019 (COVID-19) pneumonia lesions // Br J Radiol. 2021. Vol. 94, N 1122. P. 20201007. doi: 10.1259/bjr.20201007
- Avanzo M., Stancanello J., Pirrone G., et al. Radiomics and deep learning in lung cancer // Strahlenther Onkol. 2020. Vol. 196, N 10. P. 879–887. doi: 10.1007/s00066-020-01625-9
- Ji D., Zhang D., Xu J., et al. Prediction for progression risk in patients with COVID-19 pneumonia: The CALL score // Clin Infect Dis. 2020. Vol. 71, N 6. P. 1393–1399. doi: 10.1093/cid/ciaa414
- Chen H., Zeng M., Wang X., et al. A CT-based radiomics nomogram for predicting prognosis of coronavirus disease 2019 (COVID-19) radiomics nomogram predicting COVID-19 // Br J Radiol. 2021. Vol. 94, N 1117. P. 20200634. doi: 10.1259/bjr.20200634
- Wang D., Huang C., Bao S., et al. Study on the prognosis predictive model of COVID-19 patients based on CT radiomics // Sci Reports. 2021. Vol. 11, N 1. P. 11591. doi: 10.1038/s41598-021-90991-0
- Frix A.N., Cousin F., Refaee T., et al. Radiomics in lung diseases imaging: State of the art for clinicians // J Personal Med. 2021. Vol. 11, N 7. P. 602. doi: 10.3390/jpm11070602
- Murakami Y., Soyano T., Kozuka T., et al. Dose-Based radiomic analysis (dosiomics) for intensity modulated radiation therapy in patients with prostate cancer: Correlation between planned dose distribution and biochemical failure // Int J Radiat Oncol Biol Phys. 2022. Vol. 112, N 1. P. 247–259. doi: 10.1016/j.ijrobp.2021.07.1714
- Liang B., Yan H., Tian Y., et al. Dosiomics: Extracting 3D spatial features from dose distribution to predict incidence of radiation pneumonitis // Front Oncol. 2019. N 9. P. 269. doi: 10.3389/fonc.2019.00269
- Wu A., Li Y., Qi M., et al. Dosiomics improves prediction of locoregional recurrence for intensity modulated radiotherapy treated head and neck cancer cases // Oral Oncol. 2020. N 104. P. 104625. doi: 10.1016/j.oraloncology.2020.104625
- Андреев Д.А., Завьялов А.А. Критерии оценки качества лучевой терапии на примере рака предстательной железы (краткий обзор зарубежной литературы) // Проблемы социальной гигиены, здравоохранения и истории медицины. 2021. Т. 29, № S2. C. 1292–1297. doi: 10.32687/0869-866X-2021-29-s2-1292-1297
- Chen Q., Xia T., Zhang M., et al. Radiomics in stroke neuroimaging: Techniques, applications, and challenges // Aging Dis. 2021. Vol. 12, N 1. P. 143–154. doi: 10.14336/AD.2020.0421
- Mayerhoefer M.E., Materka A., Langs G., et al. Introduction to radiomics // J Nucl Med. 2020. Vol. 61, N 4. P. 488–495. doi: 10.2967/jnumed.118.222893
- Van Timmeren J.E., Cester D., Tanadini-Lang S., et al. Radiomics in medical imaging: “How-to” guide and critical reflection // Insights Imaging. 2020. Vol. 11, N 1. P. 91. doi: 10.1186/s13244-020-00887-2
- Radiomic Features: pyradiomics v3.0.1.post15+g2791e23 documentation [интернет]. Режим доступа: https://pyradiomics.readthedocs.io/en/latest/features.html#. Дата обращения: 21.04.2023.
- Al-Areqi F., Konyar M.Z. Effectiveness evaluation of different feature extraction methods for classification of COVID-19 from computed tomography images: A high accuracy classification study // Biomed Signal Process Control. 2022. N 76. P. 103662. doi: 10.1016/j.bspc.2022.103662
- Zwanenburg A., Vallières M., Abdalah M.A., et al. The image biomarker standardization initiative: Standardized quantitative radiomics for high-throughput image-based phenotyping // Radiology. 2020. Vol. 295, N 2. P. 328–338. doi: 10.1148/radiol.2020191145
- Galloway M.M. Texture analysis using gray level run lengths // Comput Graph Image Process. 1975. Vol. 4, N 2. P. 172–179. doi: 10.1016/s0146-664x(75)80008-6
- Thibault G., Angulo J., Meyer F. Advanced statistical matrices for texture characterization: application to cell classification // IEEE Trans Biomed Eng. 2014. Vol. 61, N 3. P. 630–637. doi: 10.1109/TBME.2013.2284600
- Chen S., Harmon S., Perk T., et al. Using neighborhood gray tone difference matrix texture features on dual time point PET/CT images to differentiate malignant from benign FDG-avid solitary pulmonary nodules // Cancer Imaging. 2019. Vol. 19, N 1. P. 56. doi: 10.1186/s40644-019-0243-3
- He J., Ren J., Niu G., et al. Multiparametric MR radiomics in brain glioma: Models comparation to predict biomarker status // BMC Med Imaging. 2022. Vol. 22, N 1. P. 137. doi: 10.1186/s12880-022-00865-8
- Gabryś H.S., Buettner F., Sterzing F., et al. Design and selection of machine learning methods using radiomics and dosiomics for normal tissue complication probability modeling of xerostomia // Front Oncol. 2018. N 8. P. 35. doi: 10.3389/fonc.2018.00035
- Леденев В.В., Нуднов Н.В., Сотников В.М., и др. Результаты количественной оценки постлучевых изменений в легких у онкологических пациентов, полученные с помощью новой методики анализа динамически выполненных РКТ-исследований органов грудной клетки // Вестник рентгенологии и радиологии. 2020. Т. 101, № 1. С. 30–38. doi: 10.20862/0042-4676-2020-101-1-30-38
- Леденев В.В., Солодкий В.А., Нуднов Н.В., и др. Количественные характеристики лучевого повреждения легочной ткани у онкологических пациентов при лучевой терапии на основании данных РКТ // Медицинская визуализация. 2022. Т. 26, № 4. С. 60–74. doi: 10.24835/1607-0763-1182
- Rossi L., Bijman R., Schillemans W., et al. Texture analysis of 3D dose distributions for predictive modelling of toxicity rates in radiotherapy // Radiother Oncol. 2018. Vol. 129, N 3. P. 548–553. doi: 10.1016/j.radonc.2018.07.027
- Liu J., Guo W., Zeng P., et al. Vertebral MRI-based radiomics model to differentiate multiple myeloma from metastases: Influence of features number on logistic regression model performance // Eur Radiol. 2021. Vol. 32, N 1. P. 572–581. doi: 10.1007/s00330-021-08150-y
- Dhir C.S., Lee S.Y. Discriminant independent component analysis // IEEE Trans Neural Netw. 2011. Vol. 22, N 6. P. 845–857. doi: 10.1109/TNN.2011.2122266
- Random Forest Feature Importance Computed in 3 Ways with Python / MLJAR [интернет]. Режим доступа: https://mljar.com/blog/feature-importance-in-random-forest/. Дата обращения: 21.04.2023.
- Sun R., Lerousseau M., Henry T., et al. Intelligence artificielle en radiothérapie: Radiomique, pathomique, et prédiction de la survie et de la réponse aux traitements // Cancer Radiothér. 2021. Vol. 25, N 6-7. P. 630–637. doi: 10.1016/j.canrad.2021.06.027
- Zhang X., Zhang Y., Zhang G., et al. Deep learning with radiomics for disease diagnosis and treatment: Challenges and potential // Front Oncol. 2022. N 12. P. 276. doi: 10.3389/fonc.2022.773840
- Zhang Z., Wang Z., Yan M., et al. Radiomics and dosiomics signature from whole lung predicts radiation pneumonitis: A model development study with prospective external validation and decision-curve analysis // Int J Radiat Oncol Biol Phys. 2023. Vol. 115, N 3. P. 746–758. doi: 10.1016/j.ijrobp.2022.08.047
- Li B., Ren G., Guo W., et al. Function-Wise Dual-Omics analysis for radiation pneumonitis prediction in lung cancer patients // Front Pharmacol. 2022. N 13. P. 3445. doi: 10.3389/fphar.2022.971849
- Li B., Zheng X., Zhang J., et al. Lung subregion partitioning by incremental dose intervals improves omics-based prediction for acute radiation pneumonitis in non-small-cell lung cancer patients // Cancers (Basel). 2022. Vol. 14, N 19. P. 4889. doi: 10.3390/cancers14194889
- Zhou L., Wen Y., Zhang G., et al. Machine learning-based multiomics prediction model for radiation pneumonitis // J Oncol. 2023. Vol. 2023. P. 5328927. doi: 10.1155/2023/5328927
- Kraus K.M., Oreshko M., Bernhardt D., et al. Dosiomics and radiomics to predict pneumonitis after thoracic stereotactic body radiotherapy and immune checkpoint inhibition // Front Oncol. 2023. N 13. P. 1056. doi: 10.3389/fonc.2023.1124592
- Puttanawarut C., Sirirutbunkajorn N., Khachonkham S., et al. Biological dosiomic features for the prediction of radiation pneumonitis in esophageal cancer patients // Radiat Oncol. 2021. Vol. 16, N 1. P. 220. doi: 10.1186/s13014-021-01950-y
- Liang B., Tian Y., Chen X., et al. Prediction of radiation pneumonitis with dose distribution: A convolutional neural network (CNN) based model // Front Oncol. 2020. N 9. P. 1500. doi: 10.3389/fonc.2019.01500
- Adachi T., Nakamura M., Shintani T., et al. Multi-institutional dose-segmented dosiomic analysis for predicting radiation pneumonitis after lung stereotactic body radiation therapy // Med Phys. 2021. Vol. 48, N 4. P. 1781–1791. doi: 10.1002/mp.14769
- Lee S.H., Han P., Hales R.K., et al. Multi-view radiomics and dosiomics analysis with machine learning for predicting acute-phase weight loss in lung cancer patients treated with radiotherapy // Phys Med Biol. 2020. Vol. 65, N 19. P. 195015. doi: 10.1088/1361-6560/ab8531
- Han P., Lee S.H., Noro K., et al. Improving early identification of significant weight loss using clinical decision support system in lung cancer radiation therapy // JCO Clin Cancer Inform. 2021. N 5. P. 944–952. doi: 10.1200/CCI.20.00189
- Zheng X., Guo W., Wang Y., et al. Multi-omics to predict acute radiation esophagitis in patients with lung cancer treated with intensity-modulated radiation therapy // Eur J Med Res. 2023. Vol. 28, N 1. P. 126. doi: 10.1186/s40001-023-01041-6
- Ren W., Liang B., Sun C., et al. Dosiomics-based prediction of radiation-induced hypothyroidism in nasopharyngeal carcinoma patients // Phys Medica. 2021. Vol. 89. P. 219–225. doi: 10.1016/j.ejmp.2021.08.009
- Yang S.S., OuYang P.Y., Guo J.G., et al. Dosiomics risk model for predicting radiation induced temporal lobe injury and guiding individual intensity-modulated radiation therapy // Int J Radiat Oncol Biol Phys. 2023. Vol. 115, N 5. P. 1291–1300. doi: 10.1016/j.ijrobp.2022.11.036
- Monti S., Xu T., Liao Z., et al. On the interplay between dosiomics and genomics in radiation-induced lymphopenia of lung cancer patients // Radiother Oncol. 2022. N 167. P. 219–225. doi: 10.1016/j.radonc.2021.12.038
- Kamezawa H., Arimura H. Recurrence prediction with local binary pattern-based dosiomics in patients with head and neck squamous cell carcinoma // Phys Eng Sci Med. 2022. Vol. 46, N 1. P. 99–107. doi: 10.1007/s13246-022-01201-8
- Wang B., Liu J., Zhang X., et al. Prognostic value of 18F-FDG PET/CT-based radiomics combining dosiomics and dose volume histogram for head and neck cancer // EJNMMI Res. 2023. Vol. 13, N 1. P. 14. doi: 10.1186/s13550-023-00959-6
- Pirrone G., Matrone F., Chiovati P., et al. Predicting local failure after partial prostate re-irradiation using a dosiomic-based machine learning model // J Pers Med. 2022. Vol. 12, N 9. P. 1491. doi: 10.3390/jpm12091491
- Buizza G., Paganelli C., D’Ippolito E., et al. Radiomics and dosiomics for predicting local control after carbon-ion radiotherapy in skull-base chordoma // Cancers. 2021. Vol. 13, N 2. P. 339. doi: 10.3390/cancers13020339
- Morelli L., Parrella G., Molinelli S., et al. A Dosiomics analysis based on linear energy transfer and biological dose maps to predict local recurrence in sacral chordomas after carbon-ion radiotherapy // Cancers (Basel). 2023. Vol. 15, N 1. P. 33. doi: 10.3390/cancers15010033
- Cai C., Lv W., Chi F., et al. Prognostic generalization of multi-level CT-dose fusion dosiomics from primary tumor and lymph node in nasopharyngeal carcinoma // Med Phys. 2023. Vol. 50, N 2. P. 922–934. doi: 10.1002/mp.16044
- Wang D., Lee S.H., Geng H., et al. Interpretable machine learning for predicting pathologic complete response in patients treated with chemoradiation therapy for rectal adenocarcinoma // Front Artif Intell. 2022. N 5. P. 1059033. doi: 10.3389/frai.2022.1059033
- Lam S.K., Zhang Y., Zhang J., et al. Multi-Organ omics-based prediction for adaptive radiation therapy eligibility in nasopharyngeal carcinoma patients undergoing concurrent chemoradiotherapy // Front Oncol. 2022. N 11. P. 792024. doi: 10.3389/fonc.2021.792024
- Puttanawarut C., Sirirutbunkajorn N., Tawong N., et al. Radiomic and dosiomic features for the prediction of radiation pneumonitis across esophageal cancer and lung cancer // Front Oncol. 2022. N 12. P. 768152. doi: 10.3389/fonc.2022.768152
- Puttanawarut C., Sirirutbunkajorn N., Tawong N., et al. Impact of interfractional error on dosiomic features // Front Oncol. 2022. N 12. P. 726896. doi: 10.3389/fonc.2022.726896
- Adachi T., Nakamura M., Kakino R., et al. Dosiomic feature comparison between dose-calculation algorithms used for lung stereotactic body radiation therapy // Radiol Phys Technol. 2022. Vol. 15, N 1. P. 63–71. doi: 10.1007/s12194-022-00651-9
- Sun L., Smith W., Kirkby C. Stability of dosiomic features against variations in dose calculation: An analysis based on a cohort of prostate external beam radiotherapy patients // J Appl Clin Med Phys. 2023. Vol. 24, N 5. P. e13904 doi: 10.1002/acm2.13904
- Placidi L., Gioscio E., Garibaldi C., et al. A multicentre evaluation of dosiomics features reproducibility, stability and sensitivity // Cancers (Basel). 2021. Vol. 13, N 15. P. 3835. doi: 10.3390/cancers13153835
- Placidi L., Cusumano D., Lenkowicz J., et al. On dose cube pixel spacing pre-processing for features extraction stability in dosiomic studies // Phys Medica. 2021. N 90. P. 108–114. doi: 10.1016/j.ejmp.2021.09.010
Дополнительные файлы