Частота выявления антител к вирусу Западного Нила среди пациентов с острой фебрильностью в Илорине, Нигерия
- Авторы: Odebisi-Omokanye M.B.1, Suleiman M.M.2, Sulaiman M.K.1, Atolagbe S.A.1
-
Учреждения:
- Университет Илорина
- Саммитский университет Оффа
- Выпуск: Том 69, № 4 (2024)
- Страницы: 320-328
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://ogarev-online.ru/0507-4088/article/view/265955
- DOI: https://doi.org/10.36233/0507-4088-241
- EDN: https://elibrary.ru/pvhwlc
- ID: 265955
Цитировать
Полный текст
Аннотация
Введение. Вирус Западного Нила (ВЗН), представитель семейства Flaviviridae, является одним из наиболее широко распространенных арбовирусов в мире. В развивающихся странах, таких как Нигерия, лихорадку, возникающую в результате инфекции ВЗН, часто ошибочно ассоциируют с малярией или брюшным тифом из-за неправильного диагноза и низкого уровня осведомленности об этой инфекции. В настоящем исследовании определяли распространенность антител к ВЗН классов IgM и IgG среди пациентов с лихорадкой в мегаполисе Илорин.
Материалы и методы. В общей сложности у 200 пациентов были взяты образцы крови, и каждая сыворотка была проверена на наличие антител к ВЗН классов IgM и IgG с использованием непрямого иммуноферментного анализа (ELISA). Были рассчитаны статистическая корреляция и коэффициенты логистической регрессии.
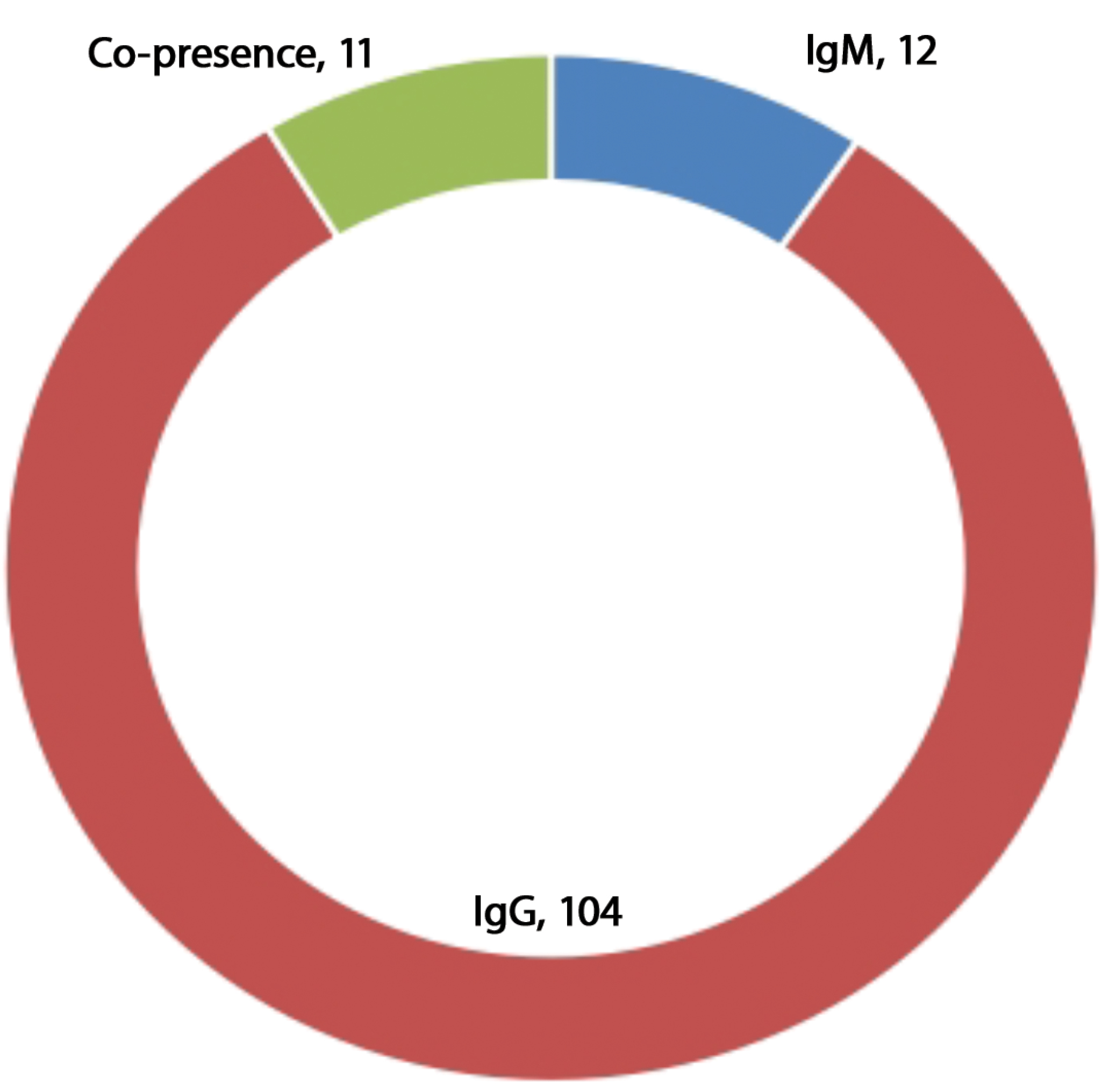
Pезультаты. В целом анти-ВЗН IgM были выявлены в 6% (12/200) пациентов с острой лихорадкой, с более высокой частотой выявления (6,30%) у женщин, чем у мужчин (5,45%).Частота выявления анти-ВЗН IgG составила 52% (104/200), при этом серопревалентность среди мужчин составила 50,67%, а среди женщин ‒ 38,95%. На стадии реконвалесценции, о которой свидетельствует одновременное обнаружение антител к ВЗН классов IgG и IgM, находились 5,4% (11/200) участников. Была получена статистически значимая корреляция серопозитивности с возрастом и религией респондентов, тогда как пол, род занятий, использование противомоскитных сеток и уровень образования не имели положительной корреляции при p < 0,05. Однако на основе отношения рисков при 95% ДИ и коэффициентов логистической регрессии такие факторы риска, как переливание крови, место проживания, инфицирование малярийным плазмодием, близость к стоячей воде и зарослям кустарника, были значимыми для положительного результата выявления анти-ВЗН-IgG и -IgM.
Заключение. Результаты этого исследования показывают циркуляцию ВЗН в исследуемой зоне. Клиницистам/врачам необходимо срочно включить скрининг на вирус Западного Нила у пациентов с лихорадкой перед началом лечения.
Ключевые слова
Полный текст
Открыть статью на сайте журналаОб авторах
Mutiat Busayo Odebisi-Omokanye
Университет Илорина
Автор, ответственный за переписку.
Email: odebisi.mb@unilorin.edu.ng
ORCID iD: 0000-0001-9825-3193
PhD (медицинская микробиология), старший преподаватель кафедры микробиологии
Нигерия, PMB 1515, ИлоринMuhammed Mustapha Suleiman
Саммитский университет Оффа
Email: Suleiman.muhammed@summituniversity.edu.ng
ORCID iD: 0000-0003-3275-1709
PhD (медицинская микробиология), преподаватель кафедры микробиологии
Нигерия, P.M.B. 4412, ОффаMariam Kehinde Sulaiman
Университет Илорина
Email: Sulaiman.km@unilorin.edu.ng
ORCID iD: 0000-0002-8295-7855
PhD (микробиология и клеточная биология), старший преподаватель кафедры медицинской микробиологии и паразитологии, Старый колледж медицинских наук
Нигерия, PMB 1515, ИлоринSidiq Abubakar Atolagbe
Университет Илорина
Email: ayinlatorla@gmail.com
ORCID iD: 0009-0007-2330-0232
аспирант кафедры микробиологии
Нигерия, PMB 1515, ИлоринСписок литературы
- Petersen L.R., Brault A.C., Nasci R.S. West Nile virus: review of the literature. JAMA. 2013; 310(3): 308–15. https://doi.org/10.1001/jama.2013.8042
- Huhtamo E., Cook S., Moureau G., Uzcátegui N.Y., Sironen T., Kuivanen S., et al. Novel flaviviruses from mosquitoes: mosquito-specific evolutionary lineages within the phylogenetic group of mosquito-borne flaviviruses. Virology. 2014; 464-465: 320–9. https://doi.org/10.1016/j.virol.2014.07.015
- Chancey C., Grinev A., Volkova E., Rios M. The global ecology and epidemiology of West Nile virus. Biomed. Res. Int. 2015; 2015: 376230. https://doi.org/10.1155/2015/376230
- Hayes E.B., Komar N., Nasci R.S., Montgomery S.P., O’Leary D.R., Campbell G.L. Epidemiology and transmission dynamics of West Nile virus disease. Emerg. Infect. Dis. 2005; 11(8): 1167–73. https://doi.org/10.3201/eid1108.050289a
- Calistri P., Giovannini A., Hubalek Z., Ionescu A., Monaco F., Savini G., et al. Epidemiology of West Nile in Europe and in the Mediterranean Basin. Open Virol. J. 2010; 4: 29–37. https://doi.org/10.2174/1874357901004020029
- Mencattelli G., Ndione M.H.D., Rosà R., Marini G., Diagne C.T., Diagne M.M., et al. Epidemiology of West Nile virus in Africa: An underestimated threat. PLoS Negl. Trop. Dis. 2022; 16(1): e0010075. https://doi.org/10.1371/journal.pntd.0010075
- Sampathkumar P. West Nile virus: epidemiology, clinical presentation, diagnosis, and prevention. Mayo. Clin. Proc. 2003; 78(9): 1137–43; quiz 1144. https://doi.org/10.4065/78.9.1137
- CDC. Blood Transfusion and Organ Donation (West Nile Virus); 2024. Available at: https://www.cdc.gov/west-nile-virus/causes/blood-transfusions.html#:~:text=Can%20I%20donate%20blood%20if,should%20tell%20your%20blood%20center
- Powell J.R. Modifying mosquitoes to suppress disease transmission: Is the long wait over? Genetics. 2022; 221(3): iyac072. https://doi.org/10.1093/genetics/iyac072
- Dahmana H., Mediannikov O. Mosquito-borne diseases emergence/resurgence and how to effectively control it biologically. Pathogens. 2020; 9(4): 310. https://doi.org/10.3390/pathogens9040310
- Pealer L.N., Marfin A.A., Petersen L.R., Lanciotti R.S., Page P.L., Stramer S.L., et al. Transmission of West Nile virus through blood transfusion in the United States in 2002. N. Engl. J. Med. 2003; 349(13): 1236–45. https://doi.org/10.1056/NEJMoa030969
- Santini M., Haberle S., Židovec-Lepej S., Savić V., Kusulja M., Papić N., et al. Severe West Nile virus neuroinvasive disease: clinical characteristics, short- and long-term outcomes. Pathogens. 2022; 11(1): 52. https://doi.org/10.3390/pathogens11010052
- Hernandez Acosta R.A., Esquer Garrigos Z., Marcelin J.R., Vijayvargiya P. COVID-19 pathogenesis and clinical manifestations. Infect. Dis. Clin. North Am. 2022; 36(2): 231–49. https://doi.org/10.1016/j.idc.2022.01.003
- Monath T.P., Arroyo J., Miller C., Guirakhoo F. West Nile virus vaccine. Curr. Drug Targets Infect. Disord. 2001; 1(1): 37–50. https://doi.org/10.2174/1568005013343254
- CDC. West Nile virus. Clinical evaluation and disease; 2024. Available at: https://www.cdc.gov/west-nile-virus/hcp/clinical-signs/?CDC_AAref_Val=https://www.cdc.gov/westnile/healthcareproviders/healthCareProviders-ClinLabEval.html
- Ma’aji J.A., Olonitola O.S., Ella E.E. Seroprevalence of West Nile virus (WNV) infection among febrile patients attending selected hospitals in Kaduna state, Nigeria. Sci. Afr. 2020; 10: e00588. https://doi.org/10.1016/j.sciaf.2020.e00588
- Abdullahi I.N., Emeribe A.U., Ghamba P.E., Omosigho P.O., Bello Z.M., Oderinde B.S., et al. Distribution pattern and prevalence of West Nile virus infection in Nigeria from 1950 to 2020: a systematic review. Epidemiol. Health. 2020; 42: e2020071. https://doi.org/10.4178/epih.e2020071
- Abdullahi I.N., Emeribe A.U., Ghamba P.E., Omosigho P.O., Bello Z.M., Oderinde B.S., et al. Distribution pattern and prevalence of West Nile virus infection in Nigeria from 1950 to 2020: a systematic review. Epidemiol. Health. 2020; 42: e2020071. https://doi.org/10.4178/epih.e2020071
- Carson P.J., Borchardt S.M., Custer B., Prince H.E., Dunn-Williams J., Winkelman V., et al. Neuroinvasive disease and West Nile virus infection, North Dakota, USA, 1999–2008. Emerg. Infect. Dis. 2012; 18(4): 684–6. https://doi.org/10.3201/eid1804.111313
- Omilabu S.A., Olaleye O.D., Aina Y., Fagbami A.H. West Nile complement fixing antibodies in Nigerian domestic animals and humans. J. Hyg. Epidemiol. Microbiol. Immunol. 1990; 34(4): 357–63.
- Udeze A.O., Shittu H.K., Ashaka O.S., Jakkari A., Oyefolu A.O. Anti-West Nile virus immunoglobulin G and M profiles of patients with Pyrexia of unknown origin In Ilorin, Nigeria. Biokemistri. 2022; 34(3): 34432–40.
- Murgue B., Murri S., Triki H., Deubel V., Zeller H.G. West Nile in the Mediterranean basin: 1950–2000. Ann. N.Y. Acad. Sci. 2001; 951: 117–26. https://doi.org/10.1111/j.1749-6632.2001.tb02690.x
- Mease L.E., Coldren R.L., Musila L.A., Prosser T., Ogolla F., Ofula V.O., et al. Seroprevalence and distribution of arboviral infections among rural Kenyan adults: a cross-sectional study. Virol. J. 2011; 8: 371. https://doi.org/10.1186/1743-422x-8-371
Дополнительные файлы