Иммунологические свойства химерного белка, содержащего основной капсидный белок echovirus 30 (Picornaviridae: Enterovirus: Enterovirus betacoxsackie)
- Авторы: Мелентьев Д.А.1, Новиков Д.В.1, Мохонова Е.В.1, Новикова Н.А.1, Кашников А.Ю.1, Селиванова С.Г.1, Голицына Л.Н.1, Лапин В.А.1, Цыганова М.И.1, Зайцев Д.Е.1, Новиков В.В.1
-
Учреждения:
- ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
- Выпуск: Том 70, № 2 (2025)
- Страницы: 189-198
- Раздел: ОРИГИНАЛЬНЫЕ ИССЛЕДОВАНИЯ
- URL: https://ogarev-online.ru/0507-4088/article/view/310657
- DOI: https://doi.org/10.36233/0507-4088-311
- EDN: https://elibrary.ru/peagdt
- ID: 310657
Цитировать
Полный текст
Аннотация
Введение. Энтеровирусная инфекция, широко распространенная в мире и в России, характеризуется разнообразием клинических форм, одной из которых является серозный менингит. Наиболее частой причиной энтеровирусного менингита у детей является вирус echovirus 30 (E30). Ранее нами получен химерный белок, состоящий из S-домена белка VP1 норовируса (SN), слитого в одну молекулу с VP1 Е30 (SN-VP1E30), который в перспективе может быть использован для разработки вакцины для профилактики энтеровирусного менингита, вызванного вирусом Е30.
Целью настоящей работы явилось изучение иммунологических свойств белка SN-VP1E30.
Материалы и методы. Мышей линии Balb/c и морскую свинку иммунизировали белком SN-VP1E30. Продукцию антител класса G (IgG) и M (IgM) исследовали методом иммуноферментного анализа. Взаимодействие антител против SN-VP1E30 с вирионами энтеровирусов Е30 разных генотипов изучали методом электронной микроскопии. Реакцию нейтрализации Е30 антителами проводили в культуре клеток RD.
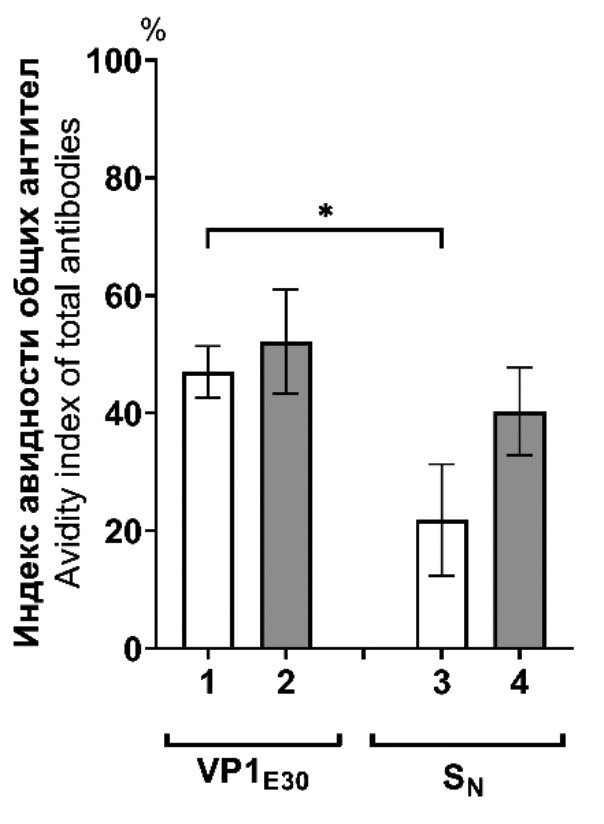
Результаты. У мышей, иммунизированных SN-VP1E30 без адъюванта, средние титры суммарных антител против VP1 E30 составили 1 : 19 000. Использование адъюванта повышало средний титр антител в 3 раза. Уровень IgM был значительно ниже и составил в среднем 1 : 1500. С помощью иммуноэлектронной микроскопии показано, что антитела морской свинки против химерного SN-VP1E30 способны связывать вирионы E30 генотипов h и еС2. Антитела мышей и морской свинки способны нейтрализовать Е30 в культуре клеток RD. У мышей титры нейтрализующих антител варьировали от 20 до 40, у морской свинки составили 40.
Заключение. Иммуногенность SN-VP1E30 у двух видов животных и способность антител связывать и нейтрализовать энтеровирус Е30 позволяет предложить его в качестве антигена в составе вакцины для профилактики заболеваний, вызванных E30.
Ключевые слова
Полный текст
Открыть статью на сайте журналаОб авторах
Дмитрий Александрович Мелентьев
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Автор, ответственный за переписку.
Email: dim-melente@yandex.ru
ORCID iD: 0000-0002-2441-6874
младший научный сотрудник лаборатории иммунохимии
Россия, 603950, г. Нижний НовгородДмитрий Викторович Новиков
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: novikov.dv75@mail.ru
ORCID iD: 0000-0001-7049-6935
канд. биол. наук, доцент, ведущий научный сотрудник лаборатории иммунохимии
Россия, 603950, г. Нижний НовгородЕкатерина Валерьевна Мохонова
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: ekaterinamohonova@yandex.ru
ORCID iD: 0000-0002-9742-7646
научный сотрудник лаборатории иммунохимии
Россия, 603950, г. Нижний НовгородНадежда Алексеевна Новикова
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: novikova_na@mail.ru
ORCID iD: 0000-0002-3710-6648
д-р биол. наук, профессор, ведущий научный сотрудник, заведующая лабораторией молекулярной эпидемиологии вирусных инфекций
Россия, 603950, г. Нижний НовгородАлександр Юрьевич Кашников
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: mevirfc@mail.ru
ORCID iD: 0000-0003-1033-7347
научный сотрудник лаборатории молекулярной эпидемиологии вирусных инфекций
Россия, 603950, г. Нижний НовгородСветлана Григорьевна Селиванова
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: svetafor22@mail.ru
ORCID iD: 0000-0002-6610-1774
канд. биол. наук, старший научный сотрудник лаборатории молекулярной эпидемиологии вирусных инфекций
Россия, 603950, г. Нижний НовгородЛюдмила Николаевна Голицына
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: lyudmila_galitzina@mail.ru
ORCID iD: 0000-0002-8064-4476
канд. биол. наук, ведущий научный сотрудник лаборатории молекулярной эпидемиологии вирусных инфекций
Россия, 603950, г. Нижний НовгородВладислав Александрович Лапин
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: fridens.95@yandex.ru
ORCID iD: 0000-0002-5905-5722
младший научный сотрудник лаборатории иммунохимии
Россия, 603950, г. Нижний НовгородМария Игоревна Цыганова
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: maria_che@mail.ru
ORCID iD: 0000-0002-2811-6844
канд. биол. наук, ведущий научный сотрудник лаборатории иммунохимии
Россия, 603950, г. Нижний НовгородДмитрий Евгеньевич Зайцев
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: mitya.zaitseff@yandex.ru
ORCID iD: 0000-0002-7663-6924
старший лаборант лаборатории иммунохимии
Россия, 603950, г. Нижний НовгородВиктор Владимирович Новиков
ФБУН «Нижегородский НИИ эпидемиологии и микробиологии им. академика И.Н. Блохиной» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (Роспотребнадзор)
Email: mbre@mail.ru
ORCID iD: 0000-0002-2449-7213
д-р биол. наук, профессор, ведущий научный сотрудник, заведующий лабораторией иммунохимии
Россия, 603950, г. Нижний НовгородСписок литературы
- Голицына Л.Н., Кашникова А.Д., Полянина А.В., Зайцева Н.Н., Михайлова Ю.М., Черепанова Е.А. Энтеровирусная (неполио) инфекция в Российской Федерации в 2023 г. В кн.: Заболеваемость, этиологическая структура и вопросы профилактики энтеровирусной (неполио) инфекции: Информационный бюллетень № 11. Нижний Новгород; 2024: 3–8. Available at: https://nniiem.ru/file/razrabotki/2024/nniiem-inf-byulleten-n-11-po-evi-za-2023-dlya-sayta-korr-oformlenie-novikova-na.pdf
- Wallace G.S., Curns A.T., Weldon W.C., Oberste M.S. Seroprevalence of poliovirus antibodies in the United States population, 2009–2010. BMC Public Health. 2016; 16: 721. https://doi.org/10.1186/s12889-016-3386-1
- Zhu R., Cheng T., Yin Z., Liu D., Xu L., Li Y., et al. Serological survey of neutralizing antibodies to eight major enteroviruses among healthy population. Emerg. Microbes Infect. 2018; 7(1): 2. https://doi.org/10.1038/s41426-017-0003-z
- Huang K.A. Structural basis for neutralization of enterovirus. Curr. Opin. Virol. 2021; 51: 199–206. https://doi.org/10.1016/j.coviro.2021.10.006
- Al-Barwani F., Donaldson B., Pelham S.J., Young S.L., Ward V.K. Antigen delivery by virus-like particles for immunotherapeutic vaccination. Ther. Deliv. 2014; 5(11): 1223–40. https://doi.org/10.4155/tde.14.74
- Chroboczek J., Szurgot I., Szolajska E. Virus-like particles as vaccine. Acta Biochim. Pol. 2014; 61(3): 531–9.
- Ye X., Ku Z., Liu Q., Wang X., Shi J., Zhang Y., et al. Chimeric virus-like particle vaccines displaying conserved enterovirus 71 epitopes elicit protective neutralizing antibodies in mice through divergent mechanisms. J. Virol. 2014; 88(1): 72–81. https://doi.org/10.1128/JVI.01848-13
- Новиков Д.В., Мелентьев Д.А., Мохонов В.В., Кашников А.Ю., Новикова Н.А., Лапин В.А. и др. Получение вирусоподобных частиц норовируса (Caliciviridae: Norovirus), содержащих белок VP1 энтеровируса Echovirus 30 (Picornaviridae: Enterovirus: Enterovirus B). Вопросы вирусологии. 2021; 66(5): 383–9. https://doi.org/10.36233/0507-4088-79 https://elibrary.ru/mkbqet
- Лапин В.А., Новиков Д.В., Мохонова Е.В., Мелентьев Д.А., Цыганова М.И., Зайцев Д.Е. и др. Получение рекомбинантного белка VP1 норовируса и его антигенные и иммуногенные свойства. Журнал микробиологии, эпидемиологии и иммунобиологии. 2024; 101(5): 661–7. https://doi.org/10.36233/0372-9311-552 https://elibrary.ru/ubmktf
- Мелентьев Д.А., Новиков Д.В., Лапин В.А., Мохонова Е.В., Цыганова М.И., Манакова Э.А. и др. Антитела к поверхностным белкам Echovirus 30 (Enterovirus, Picornaviridae) в крови жителей Нижегородской области. Инфекция и иммунитет. 2024; 14(6): 1179–86. https://doi.org/10.15789/2220-7619-BAC-16103 https://elibrary.ru/exbfif
- Nix W.A., Oberste M.S., Pallansch M.A. Sensitive, seminested PCR amplification of VP1 sequences for direct identification of all enterovirus serotypes from original clinical specimens. J. Clin. Microbiol. 2006; 44(8): 2698–704. https://doi.org/10.1128/JCM.00542-06
- Muslin C., Kain A.M., Bessaud M., Blondel B., Delpeyroux F. Recombination in enteroviruses, a multi-step modular evolutionary process. Viruses. 2019; 11(9): 859. https://doi.org/10.3390/v11090859
- Yuan J., Tang X., Yin K., Tian J., Rui K., Ma J., et al. GITRL as a genetic adjuvant enhances enterovirus 71 VP1 DNA vaccine immunogenicity. Immunol. Res. 2015; 62(1): 81–8. https://doi.org/10.1007/s12026-015-8637-1
- Foo D.G., Alonso S., Phoon M.C., Ramachandran N.P., Chow V.T., Poh C.L. Identification of neutralizing linear epitopes from the VP1 capsid protein of Enterovirus 71 using synthetic peptides. Virus Res. 2007; 125(1): 61–8. https://doi.org/10.1016/j.virusres.2006.12.005
- Collins K.A., Snaith R., Cottingham M.G., Gilbert S.C., Hill A.V.S. Enhancing protective immunity to malaria with a highly immunogenic virus-like particle vaccine. Sci. Rep. 2017; 7: 46621. https://doi.org/10.1038/srep46621
- Wu C.N., Lin Y.C., Fann C., Liao N.S., Shih S.R., Ho M.S. Protection against lethal enterovirus 71 infection in newborn mice by passive immunization with subunit VP1 vaccines and inactivated virus. Vaccine. 2001; 20(5-6): 895–904. https://doi.org/10.1016/s0264-410x(01)00385-1
- Zhou S.L., Ying X.L., Han X., Sun X.X., Jin Q., Yang F. Characterization of the enterovirus 71 VP1 protein as a vaccine candidate. J. Med. Virol. 2015; 87(2): 256–62. https://doi.org/10.1002/jmv.24018
- Xia M., Huang P., Sun C., Han L., Vago F.S., Li K., et al. Bioengineered Norovirus S60 nanoparticles as a multifunctional vaccine platform. ACS Nano. 2018; 12(11): 10665–82. https://doi.org/10.1021/acsnano.8b02776
- Zhu W., Liu Z., Zheng X., Li J., Lu K., Jiang X., et al. A broad and potent IgM antibody against tetra-EV-As induced by EVA71 and CVA16 co-immunization. Vaccine. 2021; 39(44): 6510–9. https://doi.org/10.1016/j.vaccine.2021.09.056
- Zhu W., Li J., Wu Z., Li H., Zhang Z., Zhu X., et al. Dual blockages of a broad and potent neutralizing IgM antibody targeting GH loop of EV-As. Immunology. 2023; 169(3): 292–308. https://doi.org/10.1111/imm.13629
- Голицына Л.Н., Зверев В.В., Епифанова Н.В., Сашина Т.А., Кашников А.Ю., Созонов Д.В. и др. Энтеровирусная (неполио) инфекция в Российской Федерации в 2017 г. В кн.: Заболеваемость, этиологическая структура и вопросы профилактики энтеровирусной (неполио) инфекции: Информационный бюллетень № 5. Нижний Новгород; 2018: 5–12. Available at: https://nniiem.ru/file/razrabotki/2018/byulleten-evi-2017-n5-may-18-1.pdf
- Chen D., Duggan C., Texada D.E., Reden T.B., Kooragayala L.M., Langford M.P. Immunogenicity of enterovirus 70 capsid protein VP1 and its non-overlapping N- and C-terminal fragments. Antiviral Res. 2005; 66(2-3): 111–7. https://doi.org/10.1016/j.antiviral.2005.02.004.
- Prasad B.V., Hardy M.E., Dokland T., Bella J., Rossmann M.G., Estes M.K. X-ray crystallographic structure of the Norwalk virus capsid. Science. 1999; 286(5438): 287–90. https://doi.org/10.1126/science.286.5438.287
Дополнительные файлы